藥品關(guān)聯(lián)審評審批政策進(jìn)一步明確
為落實(shí)中共中央辦公廳、國務(wù)院辦公廳《關(guān)于深化審評審批制度改革鼓勵(lì)藥品醫(yī)療器械創(chuàng)新的意見》(廳字〔2017〕42號),原食品藥品監(jiān)管總局發(fā)布了《關(guān)于調(diào)整原料藥、藥用輔料和藥包材審評審批事項(xiàng)的公告》(2017年第146號),就進(jìn)一步明確原料藥、藥用料、直接接觸藥品的包裝材料和容器與藥品制劑關(guān)聯(lián)審評審批和監(jiān)管有關(guān)事宜發(fā)出相關(guān)公告。
吸入用鹽酸氨溴索溶液上市申請獲批準(zhǔn)進(jìn)口
7月11日,韓美提交的吸入用鹽酸氨溴索溶液的上市申請(JXHS1700033)獲得國家食品藥品監(jiān)督管理局批準(zhǔn)進(jìn)口,成為國內(nèi)第一個(gè)吸入劑型的氨溴索產(chǎn)品。氨溴索因?yàn)槠潇钐底饔枚钍芘R床醫(yī)生歡迎,導(dǎo)致注射劑被廣泛用于呼吸系統(tǒng)疾病患者的霧化治療。氨溴索在國內(nèi)醫(yī)院市場約有31億元的市場規(guī)模,其中92%都是來自于注射劑型。此次韓美入用鹽酸氨溴索溶液以【兒童用藥】的理由進(jìn)入優(yōu)先審評通道,滿足了廣大兒科患者臨床需求的同時(shí),也將對氨溴索的市場格局造成顛覆性的影響。
批準(zhǔn)情況
本周國內(nèi)批準(zhǔn)生產(chǎn)1項(xiàng),批準(zhǔn)進(jìn)口4項(xiàng)。

國內(nèi)申報(bào)情況
本周CDE 承辦的受理號一共135項(xiàng)。其中,1類新藥申請臨床10項(xiàng),2 類改型新藥申請上市4項(xiàng),3類仿制藥申請2項(xiàng),4類仿制藥申請12 項(xiàng),仿制藥一致性評價(jià)12項(xiàng),境外上市化學(xué)藥品申報(bào)上市12項(xiàng)。生物制品申請上市4項(xiàng),申請臨床2項(xiàng),補(bǔ)充申請7項(xiàng)。
國內(nèi)1類新藥申報(bào)情況
國內(nèi)1類新藥申報(bào)情況
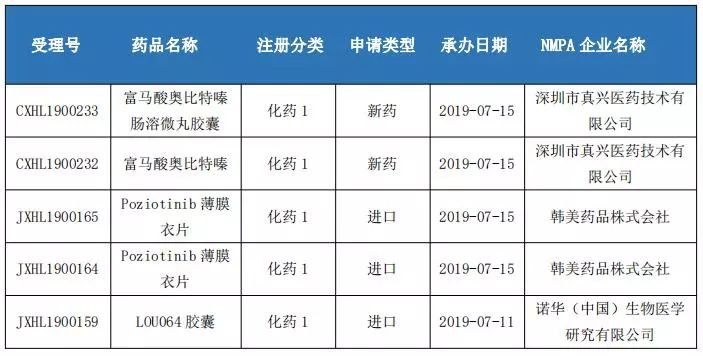
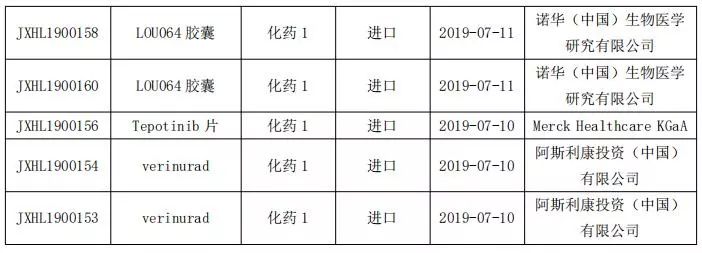
國內(nèi)改良型新藥申報(bào)情況

3、4類仿制藥申報(bào)情況




仿制藥一致性評價(jià)申報(bào)情況


境外上市藥品申請上市情況


生物制品申報(bào)情況

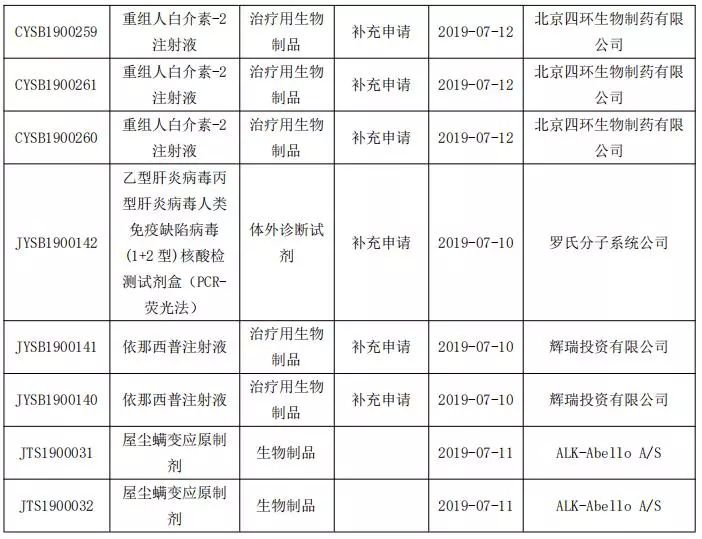
來源:Drugfocus藥研視界
注:本文為載,僅做分享之用,對文章觀點(diǎn)保持中立,侵權(quán)即刪。
