國(guó)家藥監(jiān)局(NMPA)官網(wǎng)最新顯示,安斯泰來(lái)的富馬酸吉瑞替尼片上市申請(qǐng)(受理號(hào):JXHS2000033)在2021年1月27日已處于“在審批”階段,有望于近期獲得NMPA批準(zhǔn)。每日口服1次,用于治療攜帶FLT3突?的復(fù)發(fā)性或難治性急性髓系白血病(AML)成人患者。

圖片來(lái)源:NMPA
據(jù)悉,吉瑞替尼是安斯泰來(lái)與Kotobuki制藥合作開(kāi)發(fā)的一種FMS樣酪氨酸激酶3(FLT3)抑制劑。
構(gòu)式.png)
吉瑞替尼結(jié)構(gòu)式
在2018年,吉瑞替尼相繼在日本和美國(guó)獲批上市用于治療復(fù)發(fā)性或難治性FLT3突變急性髓系白血病成年患者,它是FDA批準(zhǔn)的用于復(fù)發(fā)、難治性急性粒細(xì)胞白血病的FLT3抑制劑。
2020年4月10日,安斯泰來(lái)在中國(guó)提交的吉瑞替尼上市申請(qǐng)獲得國(guó)家藥品監(jiān)督管理局藥品審評(píng)中心(CDE)受理,并且在4月17日被擬納入優(yōu)先審評(píng),在7月30日正式納入優(yōu)先審評(píng)。距離即將獲批有不到10個(gè)月的時(shí)間。

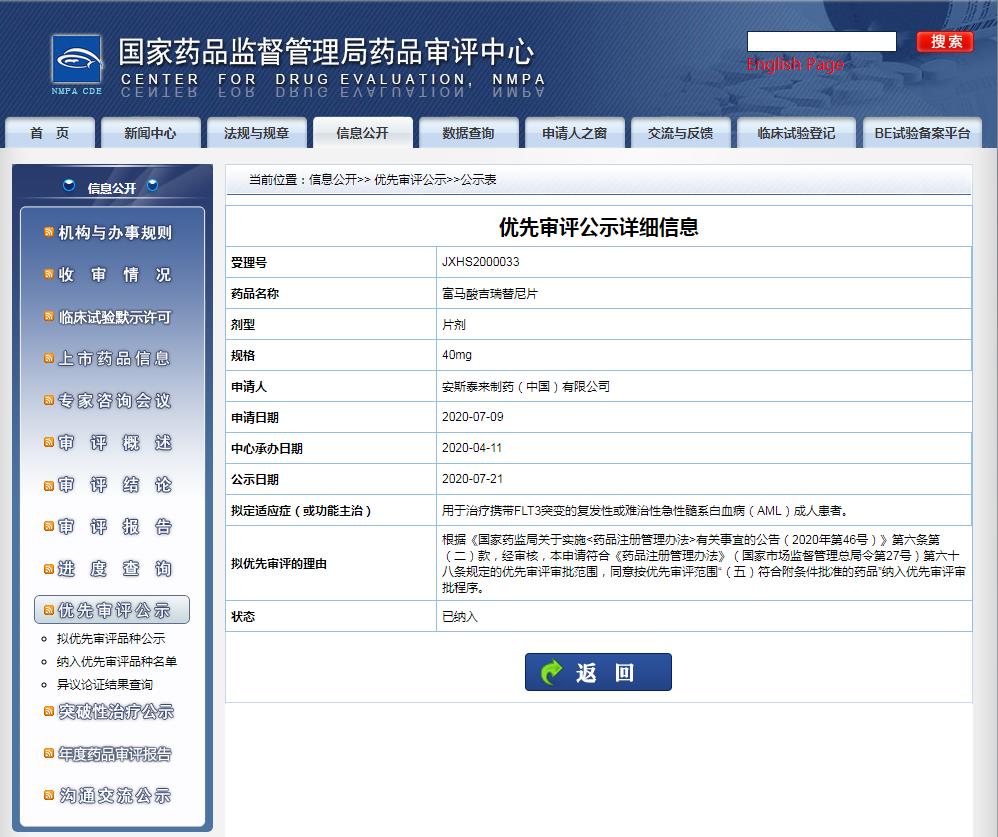
圖片來(lái)源:CDE
關(guān)于急性髓系白血病
AML:acute myelocytic leukemia,即急性髓細(xì)胞白血病,是一種影響血液和骨髓的腫瘤,發(fā)病率一般情況下會(huì)隨著年齡增長(zhǎng)而增加。據(jù)統(tǒng)計(jì),目前中國(guó)每年約有80000人診斷患有白血病[1]。急性髓系白血病的臨床表現(xiàn)一般為感染、出血、浸潤(rùn)以及貧血。特征就是骨髓里面的異常細(xì)胞快速增長(zhǎng),導(dǎo)致影響了正常細(xì)胞的產(chǎn)生,成年人一般較為容易患急性骨髓性白血病。
在過(guò)去的十年中,復(fù)發(fā)性和難治性急性髓系白血病的治療進(jìn)展較為緩慢,生存期短,并發(fā)癥多。 除了挽救性化療和造血干細(xì)胞移植以外,治療方案的選擇非常有限。
FLT3突變呈陽(yáng)性的急性髓系白血病患者預(yù)后差,化療后的生存期中位數(shù)不到6個(gè)月[2]。在急性髓系白血病的治療過(guò)程中,即使是在復(fù)發(fā)之后,F(xiàn)LT3突變的狀態(tài)有可能發(fā)生變化。因此,確認(rèn)患者FLT3的突變狀態(tài)對(duì)于確定治療方法會(huì)有幫助。
希望安斯泰來(lái)新藥「吉瑞替尼」在中國(guó)早日獲批上市,從而為急性系白血病患者帶來(lái)新的治療選擇。
參考來(lái)源:
參考來(lái)源:
[1] GLOBOCAN Cancer Today Database, International Agency for Research on Cancer, World Health Organisation.Population Fact Sheets in 2018. Available at: http://gco.iarc.fr/today/data/factsheets/populations/160-china-factsheets.pdf. Last accessed March 2020.
[2] Perl, A et al. Gilteritinib significantly prolongs overall survival in patients with FLT3-mutated (FLT3mut+) relapsed/refractory (R/R) acute myeloid leukemia (AML): Results from the Phase III ADMIRAL trial. Presented as abstract CT184 at the AACR Annual Meeting, April 22019.
